Важным элементом человеческого организма является поджелудочная железа. Наши предки называли ее железой радости, считая, что для хорошей работы этого органа нужны положительные эмоции, а стрессовые ситуации действуют разрушительно.
Поджелудочная железа выполняет несколько функций, основная из них – выделение панкреатического сока, содержащего ферменты для переваривания жиров, белков и углеводов.
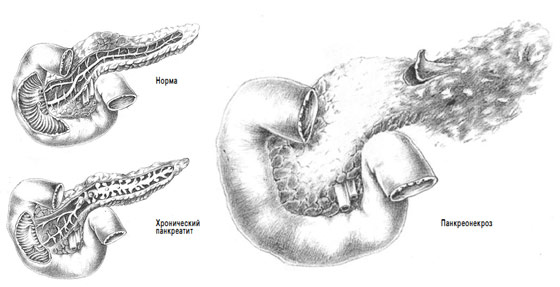
Нередко возникает воспаление поджелудочной железы, наиболее тяжелая форма которого – деструктивный панкреатит (панкреонекроз). Уникальность этого органа в том, что при панкреонекрозе пищевые ферменты активизируются в самой железе, разрушая ее ткани. Простыми словами, железа вместо пищи переваривает саму себя.
Очень важно не пропустить начало заболевания, дабы избежать опасных осложнений. Для этого надо прислушиваться к своему организму, узнавать больше о своем теле, чтобы вовремя начать профилактические и лечебные меры.
Деструктивный панкреатит: лечебно-диагностическая тактика, хирургические аспекты
Заболеваемость острым панкреатитом из года в год неуклонно растет. В структуре летальности при острых хирургических заболеваниях органов брюшной полости он занимает ведущую позицию. Этому способствуют поздняя или ошибочная диагностика, недооценка тяжести состояния больных и, соответственно, неадекватный выбор необходимых консервативных и хирургических мероприятий.
Высокий процент летальности при остром деструктивном панкреатите связан не только с биотическими изменениями, происходящими в поджелудочной железе, забрюшинной клетчатке, но и травматичностью традиционных оперативных вмешательств, число которых у одного пациента порой достигает 5–6 и более.
Принципы хирургического лечения больных панкреонекрозом основаны на дифференцированном подходе к выбору оперативных вмешательств в зависимости от фазы развития заболевания, его клинико-морфологической формы, степени тяжести состояния больного и сроков заболевания.
Различная степень распространенности некротического поражения поджелудочной железы и разных отделов забрюшинной клетчатки, а также факт их инфицирования определяют многообразие вариантов хирургической тактики.
Клинической формой острого деструктивного панкреатита (ОДП) в фазе септического расплавления и секвестрации (третья неделя от начала заболевания и более) являются инфицированный панкреонекроз и гнойно-некротический парапанкреатит различной степени распространенности.
Этот период характеризуется прогрессированием клинических и лабораторных признаков острого воспаления, повышением концентрации прокальцитонина в крови. При компьютерной томографии и УЗИ органов брюшной полости отмечают увеличение числа и размеров жидкостных образований, появление девитализированных тканей (секвестров) и/или наличие пузырьков газа. О септическом воспалении свидетельствуют и положительные результаты бактериоскопии и бактериологического посева аспирата, полученного при тонкоигольной биопсии.
Целью хирургического вмешательства при гнойных осложнениях ОДП является санация пораженной забрюшинной клетчатки. Операция включает широкое вскрытие, санацию и дренирование пораженной забрюшинной клетчатки.
Основным методом санации гнойно–некротических очагов является некро-секвестрэктомия, которая может быть как одномоментной, так и многоэтапной, при этом целесообразно использовать малоинвазивные методы (пункция и дренирование под УЗИ и КТ-наведением).
В отделении абдоминальной хирургии РКБ МЗ РТ с 2009 по 2011 гг. находилось на лечении 782 больных с острым панкреатитом. Вследствие проведения комплексной консервативной терапии 619 пациентам не потребовалось выполнение хирургического вмешательства, 163 больных были оперированы. Средний возраст составил 46,5 лет. Послеоперационная летальность составила 17,7%.
Общепризнанными показаниями к операции считают:
- инфицированный панкреонекроз;
- панкреатогенный абсцесс;
- билиарный острый деструктивный панкреатит при наличии деструктивного холецистита и/или холедохолитиаза с нарастающей желтухой и гнойным холангитом;
- травматический панкреатит при наличии полного или частичного разрыва поджелудочной железы.
Ситуация при выборе способа лечения больных со стерильным панкреонекрозом неоднозначна. Объективных критериев, позволяющих достоверно, даже во время операции определить объем некроза поджелудочной железы, до настоящего времени нет. Таким образом, показания к открытым операциям при стерильном панкреонекрозе строго ограничены. Показаны, прежде всего, малоинвазивные хирургические вмешательства: видеолапароскопия, чрескожные пункционные вмешательства.
Видеолапароскопические вмешательства с лечебно–диагностической целью были выполнены 98 пациентам, непосредственно после этих операций произошло три летальных исхода. Показания для видеолапароскопических вмешательств были следующие:
- уточнение факта панкреонекроза;
- оценка распространенности и характера панкреатогенного перитонита;
- выявление источника перитонита другой этиологии;
- ферментативный перитонит;
- выполнение лапароскопической холецистостомы;
- оментобурсостомия.
Чрескожные вмешательства под контролем УЗИ в стерильную фазу выполняли:
- при наличии отграниченных жидкостных образований забрюшинного пространства;
- для дренирования брюшной полости при ферментативном перитоните;
- для наложения холецистостомы или холангиостомы при желчной гипертензии;
- для бактериологического и биохимического исследования экссудата.
Тонкоигольное пункционное вмешательство позволяет определить наличие контаминации, оценить распространенность процесса деструкции и способствует выведению больного из эндотоксического шока.
Полученный экссудат в обязательном порядке направляется на определение уровня амилазы, микробиологическое и цитологическое исследования. Контроль за состоянием брюшной полости и забрюшинного пространства осуществляем ежедневным УЗИ, при затрудненной визуализации – РКТ или ЯМР томографией.
При проведении дренирующих перкутанных операций мы используем методы: стилет–катетер (одноэтапный), двухэтапный, троакарный. Если предполагается прохождение траектории через брюшную полость, мы применяем первые две методики.
При дренировании забрюшинного пространства без контакта с брюшной полостью предпочитаем троакарный способ, позволяющий сразу установить дренажи большого диаметра, «гильзы» ретроперитонеостомы. Через ретроперитонеостомические отверстия осуществляем осмотр, санацию забрюшинного пространства и удаление секвестров корзинкой Дормиа.
Показаниями к пункционным и дренирующим лечебным чрезкожным вмешательствам при панкреатогенных органных и внеорганных жидкостных образованиях считаем:
- жидкостные скопления в сальниковой сумке, в области селезенки и в паракольном пространстве;
- формирующиеся постнекротические псевдокисты;
- сформированные псевдокисты при наличии небольших тканевых включений и при отсутствии интерпанкреатической гипертензии;
- рецидивные и резидуальные псевдокисты и жидкостные скопления брюшной полости;
- абсцессы поджелудочной железы;
- наличие жидкости в забрюшинном пространстве;
- билиарная гипертензия.
Прежде всего пункционно-дренирующие методы применяются пациентам с инфицированным ограниченным деструктивным панкреатитом с нарастающей полиорганной недостаточностью и крайне сомнительной переносимостью операции.
Применение малоинвазивных процедур позволяет ликвидировать септические проявления и в дальнейшем выбрать более подходящее время для оперативного вмешательства в условиях наступившей демаркации некротизированных тканей.
Противопоказаниями к пункционно–дренирующему лечению являются:
- крупные секвестры в полости кисты;
- признаки кровотечения в полость кисты;
- подозрение на кистозную опухоль;
- признаки панкреатической гипертензии;
- «организованный» панкреонекроз без жидкостного компонента;
- распространенный перитонит.
Из-за неодновременного созревания секвестров после традиционных операций довольно часто формируются абсцессы, дренирование которых производится под УЗ–наведением. Траектория введения дренажа определяется с учетом адекватности оттока отделяемого, возможности замены дренажа по необходимости.
В абсцессы объемом более 60 мл устанавливаем два дренажа и более. При наличии секвестров проводим их замену на дренажи с большим просветом до 30 Fr. Большой внутренний просвет позволяет, в результате множественных промываний полостей, размывать и удалять фрагменты некротических тканей.
За 2009–2011 гг. в клинике оперированы 163 больных в различных стадиях панкреонекроза. Было выполнено около 652 пункционно–дренирующих вмешательств и около 850 процедур по замене дренажей. Пункционная санация и кратковременное дренирование проведено 27 больным.
Дренирование полости малого сальника, парапанкреатической клетчатки, паракольного пространства, тазовой клетчатки при абсцессах – 136 больным. Из них 89 больным до и 47 – после открытого оперативного лечения.
Особенно надо отметить важность РКТ-контроля. Если не удается четко определить состояние забрюшинного пространства и поджелудочной железы только при помощи УЗИ, дренирование проводим под контролем РКТ.
Инфицированные формы панкреонекроза (инфицированный панкреонекроз, панкреатогенный абсцесс, флегмона забрюшинной клетчатки, гнойный перитонит, инфицированная киста) независимо от степени полиорганных нарушений требуют оперативного лечения. В противном случае фатальный исход заболевания неизбежен.
Варианты хирургических вмешательств при инфицированном панкреонекрозе (ИП) включают в себя открытые вмешательства (лапаротомия, люмботомия) и закрытые (чрескожные вмешательства под контролем УЗИ, видеолапароскопия).
При развитии ИП, когда по результатам УЗИ, КТ установлено, что некротический компонент очага существенно преобладает над жидкостным (либо последний вовсе отсутствует), а степень тяжести состояния больного не имеет тенденции к улучшению, применение чрескожных методов дренирования ограниченно.
В наших наблюдениях было выполнено 132 открытых вмешательства по поводу инфицированного панкреонекроза. При этом основными оперативными доступами являются:
- срединная лапаротомия;
- двухподреберная лапаротомия;
- люмботомия;
- срединная лапаротомия с синхронной люмботомией.
После выполнения лапаротомии основное внимание должно быть уделено оценке распространенности и характера поражения поджелудочной железы, всех отделов забрюшинной клетчатки, органов брюшной полости.
Однако одномоментная санация у части больных с инфицированным панкреонекрозом не всегда удается, требуются повторные вмешательства, так называемые программируемые санации. Клинический смысл разделения санаций на этапы основывается на следующих положениях:
- факт неодновременного созревания секвестров;
- вторичное прогрессирование гнойного процесса по типу затеков;
- большая опасность септического шока при одномоментном раскрытии обширных забрюшинных нагноений.
Программируемые санации выполняли в режиме 24–72 часа или «по требованию», т.е. при возникновении экстренных показаний.
Источник: http://www.healthynation.ru/index.php?view=article&id=534
Лечение острого деструктивного панкреатита в ферментативную фазу заболевания
Актуальность темы.
Лечение деструктивных форм острого панкреатита остается наиболее сложной и трудоемкой проблемой для специалистов ургентной хирургии и интенсивной терапии.
Основными причинами летальных исходов от ОДП служат:
- эндотоксиновый шок и полиорганная недостаточность (так называемая «ранняя» смерть, наступающая в первую неделю заболевания);
- гнойные осложнения (ГО), в том числе сепсис («поздняя» смерть, обычно на 3-4-й неделе от начала ОДП).
Наличие нескольких «пиков» летальности от ОДП объясняется фазовым течением патологического процесса, описанного в 70-х гг. основоположником петербургской панкреатологической школы профессором В.И. Филиным.
Согласно теории фазового течения в основе ОДП лежит первичный асептический некроз поджелудочной железы (ферментативная фаза) с последующей воспалительной реакцией (реактивная фаза) и секвестрацией очагов некроза, протекающей либо асептически, либо в условиях гнойно-гнилостной инфекции.
Лечение острого деструктивного панкреатита должно начинаться с комплексной, патогенетической, консервативной терапии, направленной на подавление секреции активных ферментов поджелудочной железы, купирование синдрома токсемии активной детоксикацией, профилактику вторичной инфекции, посиндромное лечение органных дисфункций.
Однако, частое отсутствие эффекта от консервативной терапии острого деструктивного панкреатита заставляет проводить поиск новых патогенетически обоснованных методов лечения с помощью лекарственных средств целенаправленного действия.
В первую фазу ОДП лечебные мероприятия должны быть направлены в первую очередь на борьбу с эндотоксиновым шоком. В настоящее время представляет научный и практический интерес для этой цели раствор натрия гипо-хлорита – мощное средство полинаправленного действия окислительной природы, донор активного кислорода, широко и успешно применяется при лечении экзо- и эндотоксикозов, связанных с печеночно-почечной недостаточностью, отравлениями, ожогами, сепсисом и другими критическими состояниями.
Однако, действие гипохлорита натрия недостаточно изучено при лечении острого деструктивного панкреатита в ферментативную фазу. Поэтому изучение этого влияния гипохлорита натрия при остром деструктивном панкреатите в ферментативную фазу представляет определенный интерес.
Назначение антибиотиков при верифицированном диагнозе острого деструктивного панкреатита является обязательным и не вызывает сомнения, так как антибиотикотерапия ведет к профилактике инфицирования асептического некроза поджелудочной железы.
В данном случае необходим препарат широкого спектра действия, действующий бактерицидно на грамположительные и грамотрицательные микроорганизмы, устойчивые к пе-нициллинам и другим противомикробным средствам, хорошо проникающий в ткани и жидкости организма, длительно в них задерживающийся.
Использование в нашей работе препарата цефалоспоринов 3-го поколения – цефотаксима, с выше перечисленных позиций представляется оправданным, так как препарат обладает оптимальным соотношением цены и качества (при парентеральном введении цефотаксима достигается подавляющая концентрация этого препарата в тканях поджелудочной железы, он удобен в использовании- 2 инъекции в сутки и относительно дешев).
Из литературы известно, что гипохлорит натрия обеспечивает снижение резистентности микрофлоры к антибиотикам. А сочетание его с антибиотиком – цефотаксимом, очень разумно, так как увеличивается бактерицидная способность последнего. Таких данных мы ранее в литературе не встречали.
Физиотерапевтические методы (в частности постоянный ток) используются преимущественно при лечении хронических форм панкреатита. Использование постоянного (гальванического) тока в комплексной терапии острого панкреатита не нашло должного отражения в литературе.
Этому вопросу посвящены единичные публикации, касающиеся эффективности лекарственного внутритканевого электрофореза с достаточно аргументированным объяснением возможности широкого использования постоянного (гальванического) тока при остром воспалении поджелудочной железы. Авторами впервые был использован внутритканевой электрофорез поджелудочной железы при остром панкреатите в эксперименте и клинике.
Оперативное лечение острого деструктивного панкреатита преследует цель не столько купировать острый приступ болезни, сколько создать условия, позволяющие исключить вместе с консервативным лечением рецидив панкреатита и не допустить летального исхода в связи с местными осложнениями.
Ранние оперативные вмешательства направлены на ликвидацию разлитого перитонита и оментобурсита, уменьшение отечно-воспалительных изменений в забрюшинной клетчатке вокруг поджелудочной железы, а также в самой железе, на снятие гипертензии в желчевыводящих путях и панкреатических протоках.
Существующие способы лечения острого деструктивного панкреатита с помощью лапароскопического дренирования брюшной полости при тяжелой степени интоксикации, распространенном панкреатогенном перитоните не лишены недостатков, которые приводят в конечном итоге к развитию гнойных осложнений и летальным исходам.
К таким недостаткам, на наш взгляд, относятся невозможность одномоментной адекватной лапароскопической санации брюшной полости и короткое (24 – 48 часов) действие дренирующей способности поставленных дренажей, что заставляет врачей выполнять релапароскопи-ческое дренирование брюшной полости.
Неполное же удаление панкретоген-ного выпота из брюшной полости, как «вторичного депо» токсинов, сохраняет выраженность эндогенной интоксикации, которая может привести к летальному исходу.
Разработка новых и усовершенствование известных способов лечения острого деструктивного панкреатита с применением лапароскопических вмешательств, лишенных вышеперечисленных недостатков, представляется перспективным направлением в решении задач по улучшению результатов лечения больных острым деструктивным панкреатитом.
Цель исследования
Улучшить результаты лечения больных острым деструктивным панкреатитом в ферментативную фазу заболевания путем применения внутритканевого электрофореза поджелудочной железы с раствором гипохлорита натрия и усовершенствования методики лапароскопического дренирования брюшной полости.
Задачи исследования
- Изучить эффективность сочетанного применения раствора гипохлорита натрия и гальванизации поджелудочной железы при остром деструктивном панкреатите в ферментативную фазу заболевания.
- Разработать и изучить эффективность лечения ферментативного перитонита путем лапароскопического дренирования брюшной полости новыми дренажными устройствами в сочетании с перитонеальным лаважем.
- Оценить результаты лечения больных острым деструктивным панкреатитом при использовании разработанных миниинвазивных технологий в ферментативную фазу заболевания.
Научная новизна
Разработан и внедрен в клинику новый эффективный метод комплексного консервативного лечения острого деструктивного панкреатита в ферментативную фазу заболевания с направленным применением раствора гипохлорита натрия и гальванизации поджелудочной железы.
Предложен метод закрытого лечения ферментативного перитонита при остром деструктивном панкреатите с использованием малоинвазивных технологий (лапароскопическое дренирование брюшной полости устройствами, обеспечивающими мелкодисперсный гидропрессивный поток гипохлорита натрия в сочетании с перитонеальным лаважем). Изучены и оценены результаты лечения больных острым деструктивным панкреатитом при использовании разработанных технологий в ферментативную фазу заболевания.
Практическая ценность
Включение в комплекс лечебных мероприятий при остром деструктивном панкреатите в ферментативную фазу внутритканевого электрофореза поджелудочной железы с раствором гипохлорита натрия способствует уменьшению эндогенной интоксикации, предупреждению прогрессирования патологического процесса и сокращению сроков лечения.
Сочетанное применение лапароскопического дренирования брюшной полости устройством, обеспечивающим мелкодисперсный гидропрессивный поток гипохлорита натрия и перитонеального лаважа способствует уменьшению эндогенной интоксикации, гнойных осложнений, сокращению сроков лечения и снижению летальности больных острым деструктивным панкреатитом, осложненным ферментативным перитонитом.
Основные положения, выносимые на защит
- Включение в комплекс лечебных мероприятий при остром деструктивном панкреатите в ферментативную фазу внутритканевого электрофореза поджелудочной железы с раствором гипохлорита натрия помогает эффективно снизить панкреатогенную интоксикацию, способствует предупреждению прогрессирования патологического процесса и служит профилактикой гнойных осложнений.
- Закрытый метод лечения ферментативного перитонита при ОДП с использованием малоинвазивных технологий (лапароскопическое дренирование брюшной полости устройствами, обеспечивающими мелкодисперсный гидропрессивный поток гипохлорита натрия в сочетании с пери-тонеальным лаважем) позволяет предупредить прогрессирование панкре-онекроза, способствует уменьшению гнойных осложнений, сокращению сроков лечения и снижению летальности.
Апробация работы
Результаты исследования доложены:
- 68-я межвузовская научная конференция студентов и молодых ученых (г. Курск, 2003).
- Межрегиональная научно-практическая гастроэнтерологическая конференция (г. Курск, 2003).
- 7-ой Международный конгресс по эндоскопической хирургии (г. Москва, 2003).
- II Всероссийская конференция общих хирургов (г. Ростов, 2003).
- Всероссийская конференция «Актуальные проблемы медицины и биологии» (г. Томск, 2004).
- Научная конференция КГМУ и сессия Центрально-Черноземного научного центра РАМН, посвященная 70-летию КГМУ «Университетская наука: взгляд в будущее» (г. Курск, 2005).
- Юбилейная межвузовская научная конференция студентов и молодых . ученых, посвященная 70-летию КГМУ. Молодежная наука и современность (Курск, 2005).
- При выполнении научно-исследовательской работы оформлено семь рационализаторских предложений и получен патент на изобретение (№ 2248226 от 15.03.05).
Объем и структура диссертации
Диссертация изложена на 106 страницах машинописного текста, состоит из введения, 3-х глав, заключения, выводов, практических рекомендаций. Указатель литературы включает 121 источник (89 отечественных и 32 зарубежных). Диссертация содержит 9 рисунков и 21 таблицу.
Заключение диссертации по теме “Xирургия”, Стельмах, Евгений Николаевич
Выводы
- Включение в комплекс лечебных мероприятий внутритканевого электрофореза поджелудочной железы с раствором гипохлорита натрия у больных острым деструктивным панкреатитом в ферментативную фазу служит профилактикой гнойно-некротических осложнений, приводит к быстрому купированию болевого и интоксикационного синдромов, сокращению сроков лечения на 5 койко-дней, способствует повышению эффективности консервативного лечения в 1,6 раза и ограничению или «обрыву» патологического процесса в поджелудочной железе.
- Применение лапароскопического дренирования брюшной полости у больных с ферментативным перитонитом новыми дренажными устройствами в сочетании с перитонеальным лаважем эффективно снижает эндогенную интоксикацию, среднее пребывание больных в стационаре на 18 койко-дней и послеоперационную летальность в 1,6 раза.
- Разработанные миниинвазивные технологии лечения деструктивного панкреатита позволяют снизить общую летальность с 11,5% до 4% и количество гнойных осложнений в 2,0 раза.
Практические рекомендации
- Лечение больных острым деструктивным панкреатитом в фазу панкреа-тогенного шока и токсемии необходимо начинать с комплексной консервативной терапии, включая внутритканевой электрофорез поджелудочной железы (поперечное расположение прокладок, сила тока – 0,05 мА/см , в течение 60 минут) с 0,03-0,06% раствором гипохлорита натрия – 400 мл 1 раз в сутки в сочетании с антибиотиком — цефотаксимом (1 г цефотакси-ма вводится внутримышечно за 30 минут до проведения гальванизации поджелудочной железы).
- Для лечения больных острым деструктивным панкреатитом, осложненным ферментативным перитонитом, рекомендуется лапароскопическое дренирование брюшной полости новыми дренажными устройствами, обеспечивающими мелкодисперсный гидропрессивный поток лекарственного вещества. В послеоперационном периоде проводится перитоне-альный лаваж раствором гипохлорита натрия (0,06% раствор ЫаСЮ – 2-3 л, 1-2 раза в сутки).
Источник: http://www.dissercat.com/content/lechenie-ostrogo-destruktivnogo-pankreatita-v-fermentativnuyu-fazu-zabolevaniya
Диагностика и хирургическое лечение больных деструктивным панкреатитом
В статье отмечена актуальность проблемы лечения острого панкреатита, приведены современные классификации заболевания. Рассматриваются принципы хирургического лечения больных панкреонекрозом, показания к открытым операциям, лапаротомное хирургическое вмешательство и применение малоинвазивных технологий.
Ранняя диагностика и выбор оптимальных методов лечения больных панкреонекрозом являются одной из сложных и окончательно нерешенных проблем хирургии. Несмотря на определенные успехи, достигнутые в последнее десятилетие, летальность остается высокой и составляет от 12 до 40%.
Прогноз исхода заболевания зависит от объема поражения поджелудочной железы (ПЖ), забрюшинной клетчатки, наличия инфекции. При этом в патологический процесс вовлекаются различные органы и системы, приводя к развитию органной или полиорганной недостаточности. Высокий уровень летальности, отсутствие единой тактики побуждает хирургов к поиску наиболее оптимальных вариантов лечения больных панкреонекрозом.
Принципы хирургического лечения больных панкреонекрозом основаны на дифференцированном подходе к выбору оперативных вмешательств в зависимости от фазы развития заболевания, клинико-морфологической его формы, степени тяжести состояния больного и сроков заболевания.
Это касается показаний к операции, сроков хирургического вмешательства, последовательности применения транскутанных, лапароскопических и лапаротомных методик. Высокий процент летальности связан не только с биотическими изменениями, но и с травматичностью традиционных оперативных вмешательств, число которых у одного пациента достигает 5-6 и более.
В структуре основных нозологических форм больные с острым панкреатитом (ОП) традиционно занимают третье место после острого холецистита и острого аппендицита. По темпам роста заболеваемости острый панкреатит опережает все другие неотложные заболевания органов брюшной полости: по мировым статистическим данным, варьирует от 200 до 800 пациентов на 1 млн человек населения в год. В 25-30% случаев развитие острого панкреатита носит деструктивный характер, именно эта часть пациентов обеспечивает высокую общую и послеоперационную летальность.
В последние десятилетия произошли существенные изменения не только в диагностике и лечении острого панкреатита, но и в его классификации. В России наибольшее распространение получили классификации В.С. Савельева (1983 г.) и «Атланта» (1992 г).
По классификации, принятой в Атланте, рекомендовано выделять следующие клинические формы заболевания:
- Отечный (интерстициальный) панкреатит.
- Стерильный панреонекроз.
- Инфицированный панкреонекроз.
- Панкреатогенный абсцесс.
- Псевдокиста, ложная киста (инфицированная).
По степени тяжести заболевания выделяют всего две градации:
- Панкреатит средней степени тяжести.
- Панкреатит тяжелой степени.
По осложнениям: местные и системные.
Местные осложнения в стерильную фазу:
- парапанкреатический инфильтрат;
- асептическая (некротическая) флегмона забрюшинной клетчатки;
- ферментативный перитонит;
- аррозивные кровотечения (внутрибрюшные, желудочно-кишечные).
В инфицированную фазу:
- забрюшинная флегмона;
- панкреатический, парапанкреатический абсцесс;
- гнойный перитонит;
- желудочные, кишечные свищи;
- аррозивные кровотечения (внутрибрюшные, желудочно-кишечные).
Системные осложнения:
- панкреатогенный шок в стерильную фазу;
- инфекционно-токсический шок при инфицированном панкреонекрозе;
- синдром полиорганной недостаточности;
- тромбоэмболические осложнения.
Первичный протокол диагностики и тактики при остром панкреатите. Выполняется в приемном отделении.
Обязательно:
- Общий анализ крови с подсчетом числа тромбоцитов.
- Общий анализ мочи, диастаза мочи.
- Группа крови, резус-фактор.
- ИФЛ (антитела к Treponema Pallidum), HBsAg, a-HCV, ВИЧ.
- Биохимический анализ крови (общий белок, амилаза крови, липаза крови, креатинин, сахар крови, билирубин связанный и несвязанный, электролиты).
- Коагулограмма (протромбин, АЧТВ, фибриноген).
Инструментальные методы обследования:
Обязательно:
- ЭКГ.
- Рентгенологическое исследование грудной клетки и брюшной полости.
- УЗИ органов брюшной полости и забрюшинного пространства.
- ЭГДС (с обязательным осмотром большого дуоденального сосочка).
- КТ органов брюшной полости и забрюшинного пространства.
1. Основанием для установления диагноза острого панкреатита (после исключения другой хирургической патологии) является сочетание минимум двух следующих выявленных признаков:
- типичная клиническая картина (интенсивные некупируемые спазмолитиками боли опоясывающего характера, неукротимая рвота, вздутие живота, употребление алкоголя, острой пищи или наличие ЖКБ в анамнезе и др.);
- УЗИ (увеличение размеров, снижение эхогенности, нечеткость контуров поджелудочной железы, наличие свободной жидкости в брюшной полости);
- лабораторные показатели (гиперамилаземия, гиперамилазурия);
- высокая активность амилазы ферментативного экссудата (в 2-3 раза превышающая активность амилазы крови), полученного при пункции под контролем УЗИ;
- лапароскопические признаки острого панкреатита.
2. Диагностика острого панкреатита должна обязательно включать определение тяжести и прогноза заболевания (табл. 1), степени эндогенной интоксикации (табл. 2, 3) и оценку общего состояния пациента в динамике и по различным интегральным схемам (APACHE II, Ranson и др.).
3. Интенсивный болевой синдром, не купируемый наркотическими анальгетиками, быстро прогрессирующая желтуха, отсутствие желчи в ДПК при ФГДС, признаки билиарной гипертензии, по данным УЗИ, свидетельствуют о наличии вклиненного камня большого дуоденального сосочка (БДС).
В этом случае пациент нуждается в срочном восстановлении пассажа желчи и панкреатического сока, оптимальным методом которого служит эндоскопическая папилосфинктеротомия (ЭПСТ). При вклиненном камне БДС и остром панкреатите ЭПСТ производится без эндоскопической ретроградной холангиопанкреатографии (ЭРХПГ).
4. Оптимальным видом лечения острого панкреатита (ОП) в ферментативной фазе является интенсивная консервативная терапия.
Таблица 1
Определение тяжести и прогноза заболевания
| Клинические признаки | Оценка в баллах |
| Госпитализация в срок до 6 часов | 0,5 балла |
| Распирающие боли в спине | 0,5 балла |
| Для снятия боли требуются наркотические препараты | 0,5 балла |
| Многократная рвота без облегчения | 0,5 балла |
| Эпизоды слабости и головокружения | 1 балл |
| Бледная и серая кожа | 0,5 балла |
| Мраморность кожи и цианоз | 1,0 балл |
| Психическая заторможенность | 0,5 балла |
| Возбуждение, делирий | 1,0 балл |
| Олигурия менее 200 мл /сутки | 1,0 балл |
| Холодные кисти и стопы | 0,5 балла |
| Парез кишечника в первые 12 часов | 1,0 балл |
| Лейкоцитоз 1 6000/л и выше | 1,0 балл |
| Глюкоза крови более 10 ммоль/л | 1,0 балл |
| Креатинин крови выше 200 мкмоль/л | 1,0 балл |
| Билирубин крови выше 40 мкмоль/л, без признаков холедохолитиаза | 1,0 балл |
| Температура в подмышечной области < 36,0 | 0,5 балла |
- Сумма баллов 0 — панкреатит отсутствует или «потенциально легкий».
- Сумма баллов менее 1 — панкреатит «потенциально легкий» (состояние больного без интенсивной терапии не ухудшится), допустимо лечение в хирургическом стационаре.
- Сумма баллов 1-2 — «потенциально тяжелый» (состояние больного без интенсивной терапии будет ухудшаться — подлежит переводу в ОРИТ).
- Сумма баллов 2-6 — тяжелый ОП с плохим прогнозом (перевод в ОРИТ).
- Сумма баллов более 6 — летальный вариант панкреонекроза (перевод в ОРИТ).
Таблица 2
Определение степени тяжести ферментативной интоксикации при остром панкреатите (В.С. Савельев, 1997 г.)
| Степень тяжести | Легкая (1-2 балла) соответствует отечному панкреатиту, мелкоочаговому панкреонекрозу | Средняя (2-3 балла) соответствует крупноочаговому панкреонекрозу | Тяжелая (4-5 баллов) соответствует субтотальному и тотальному панкреонекрозу |
| Частота пульса |
< 100 |
100-120 |
>120 |
| Артериальное давление |
>120 |
100-120 |
<100 |
| Частота дыхания |
16-20 |
21-26 |
>26 |
| Диурез (л/сутки) |
1-1,5 |
0,5-1,0 |
<0,5 |
| Госпитализация | Хирургическое отделение | Палаты реанимации и интенсивной терапии | |
Таблица 3.
Оценка тяжести физиологического состояния при панкреонекрозе (ТФС)
| Признаки | 4 | 3 | 2 | 1 | 0 | 1 | 2 | 3 | 4 | |
| Пульс в минуту |
>190 |
150-189 |
80-149 |
69-79 |
55-69 |
40-54 |
<40 |
|||
| САД |
>190 |
150-189 |
80-149 |
55-79 |
<55 |
|||||
| Вазопрессоры |
Да |
|||||||||
| Температура тела |
>41 |
39-40,9 |
38-39 |
36-38 |
34-35 |
32-33 |
30-31 |
<30 |
||
| ЧД |
>50 |
35-49 |
25-34 |
12-24 |
10-11 |
6-9 |
<6 |
|||
| ИВЛ |
Да |
|||||||||
| Диурез л/сут |
>5 |
3,5-4,9 |
0,7-3,4 |
0,2-0,4 |
<0,2 |
|||||
| Сознание |
Эйфория |
Сопор |
Кома |
|||||||
| Отделяемое по назогастральному зонду |
Нет |
До 0,5 |
0,5-1 |
> 1 |
||||||
| Перистальтика |
Да |
Нет |
||||||||
| Стимуляция кишечника |
Нет |
Да |
||||||||
| Стул |
Да |
Нет |
||||||||
| ЦВД. см вод. ст. |
<0 |
1-4 |
4-16 |
> 16 |
||||||
- 0-3 — легкая степень (отечный панкреатит)
- 4-7 — средняя степень тяжести
- 8-11 — тяжелая степень
- 12 и более — крайне тяжелая степень
Основные принципы интенсивной терапии острого панкреатита, целью которых является уменьшение дальнейшей деструкции и предотвращение развития гнойных осложнений, включают в себя:
- интенсивная терапия, направленная на восстановление объема циркулирующей крови, регидратация, гемокоррекция;
- блокада секреторной функции поджелудочной железы (препараты соматостатина, антиметаболиты);
- ингибирование биологически активных веществ за счет введения ингибиторов протеаз, антигистаминных препаратов, нестероидных противовоспалительных препаратов;
- антибактериальная профилактика и терапия. Основой выбора препаратов являются данные микробиологического исследования. Спектр действия выбираемых препаратов должен охватывать грамотрицательные и грамположительные аэробные и анаэробные микроорганизмы — возбудители панкреатогенной инфекции (таблица 4);
- эндоскопическая установка назогастроинтестинального зонда за связку Трейтца для декомпрессии и энтерального питания;
- адекватная аналгезия, продленная перидуральная анестезия;
- спазмолитическая терапия;
- антикоагулянтная терапия;
- превентивная противоязвенная терапия;
- адекватная нутритивная поддержка;
- лечебно-диагностическая лапароскопия с санацией и дренированием брюшной полости, при необходимости — полости малого сальника и желчевыводящих путей;
- своевременное хирургическое лечение инфицированного панкреонекроза.
Таблица 4
Стартовая эмпирическая терапия инфекций брюшной полости в зависимости от вероятных возбудителей с ранжированием по уровню достоверности (доказательности)
| Вероятные возбудители | Бактерии группы кишечной палочки (E. coli, K. pneumonia) 17-35%Синегнойная палочка 11-16%
Стафилококки (S. aureus, S. epidermidis) 10-15% Энтерококки 10-15% Грибы 5-15% Анаэробы 5-15% Диллинджер Э.П. Инфекционные осложнения панкреатита / Клиническая микробиология и антимикробная химиотерапия. — 2003. — № 2. — Т. 5 — С.108-116. |
||
|
Стартовая терапия |
Альтернативная терапия |
Длительность |
|
| Имипенем/циластатин
по 0,5 г 4 раза в сутки в/в |
Цефепим в/в
по 1-2 г 2-3 раза в сутки + метронидазол в/в по 0,5 г 2-3 раза в сутки |
по динамике симптомов | |
| Меропенемпо 0,5-1 г 3 раза в сутки в/в
Villatoro E, Larvin M, Bassi C. Antibiotic therapy for prophylaxis against infection of pancreatic necrosis in acute pancreatitis. The Cochrane Database of Systematic Reviews 2003, Issue 4. Ципрофлоксацин в/ в по 200-400 мг 2 раза в сутки (офлоксацин или другие фторхинолоны) + метронидазол в/в по 0,5 г 2-3 раза в сутки |
Цефтазидим в/м или в/впо 1-2 г 2-3 раза в сутки
+ метронидазол в/в по 0,5 г 2-3 раза в сутки |
по динамике симптомов | |
Инфекционные осложнения при легком и среднетяжелом остром панкреатите развиваются у 2-7% пациентов. Частота инфекционных осложнений коррелирует с тяжестью заболевания. Несмотря на то, что при остром панкреатите антибиотики часто применяют, их значение в лечении этого заболевания в настоящее время не доказано.
В ранних исследованиях, отвечающих требованиям доказательной медицины, не было выявлено влияния профилактического применения антибиотиков при остром панкреатите на смертность и частоту инфекционных осложнений. Это связывают с тем, что в исследование были включены пациенты с легким и среднетяжелым течением заболевания.
В последнем систематическом обзоре у пациентов с тяжелым течением — панкреонекрозом (наличие некротизированных тканей по результатам компьютерной томографии) профилактическое назначение антибиотиков (цефуроксим, офлоксацин, имипенем/циластатин, меропенем) приводило к значительному снижению частоты развития инфицированного некроза и смертности. Авторы делают заключение, что профилактическое применение антибиотиков у таких пациентов необходимо.
Протокол лечения нетяжелого острого панкреатита
1. При госпитализации в хирургическое отделение для лечения нетяжелого панкреатита достаточно проведения базисного лечебного комплекса:
- голод;
- зондирование и аспирация желудочного содержимого;
- инфузионная терапия (солевые растворы, глюкоза) не менее 2,5-3,0 литров под контролем диуреза;
- анальгетики (НПВП);
- спазмолитики;
- блокаторы протонной помпы, Н2-блокаторы;
- ингибиторы протеолитических ферментов — апротинины (Гордокс, Контрикал) при высокой сохраняющейся гиперферментемии (разовая доза 500 000 тыс. в/в и далее 50 000 через час);
- Октреотид (Сандостатин) 100 мкг х 3 раза в сутки подкожно;
- дистигмина бромид (Убретид 0,5-1,0 1 раз в сутки по показаниям);
с целью профилактики гнойных осложнений и при мелкоочаговом панкреонекрозе:
- пефлоксацин (абактал) 400 мг 2 раза в сутки в/в капельно;
- ципрофлоксацин 200-400 мг 2 раза в сутки в/в капельно;
- офлоксацин 200 мг 2 раза в сутки в/в капельно в комбинации с метронидазолом 500 мг (100 мл) 3 раза в сутки в/в капельно.
2. При отсутствии эффекта от проводимой базисной терапии в течение 6 часов и наличии хотя бы одного из признаков тяжелого панкреатита следует констатировать тяжелый панкреатит, перевести больного в отделение реанимации и интенсивной терапии и проводить лечение, соответствующее тяжелому острому панкреатиту.
Протокол интенсивной терапии тяжелого панкреатита
Основной вид лечения — интенсивная консервативная терапия. Приведенный выше базисный лечебный комплекс при тяжелом ОП является недостаточно эффективным и должен быть дополнен специализированным лечебным комплексом. Эффективность последнего максимальна при раннем начале лечения (первые 12 часов от начала заболевания).
Хирургическое вмешательство в виде лапаротомии показано лишь при развитии осложнений хирургического профиля, которые невозможно устранить эндоскопическими методами (деструктивный холецистит, желудочно-кишечное кровотечение, острая кишечная непроходимость и др.).
Специализированное лечение:
- голод, дренирование желудка;
- катетеризация центральной вены и мочевого пузыря;
- инфузионно-трансфузионная терапия в объеме не менее 40 мл/кг массы тела при соотношении коллоидных и кристаллоидных растворов 1:4.
- Обезболивание:
- Антисекреторная терапия:
- Профилактика гнойных осложнений:
- Детоксикация:
а. перидуральная блокада на уровне Th 7-9 (метод выбора: постоянная инфузия 0,2%-ным раствора наропина со скоростью 6-12 мл/час);
б. нестероидные противовоспалительные средства (кетопрофен 100 мг 3 раза в сутки).
а. препараты выбора — Октреотид (Сандостатин) по 100 мкг 3 раза в сутки подкожно;
б. противоязвенная терапия (лосек, квамател до 120 мг в сутки в/в).
Антиферментная терапия (при наличии гиперферментемии):
а. контрикал не менее 50 000 ед./сут;
б. гордокс не менее 500 000 ед./сут.
а. пефлоксацин по 400 мг 2 раза в сутки в/в + метронидазол по 500 мг 3 раза в сутки в/в;
б. при признаках вторичного инфицирования: цефоперазон/сульбактам, цефепим, имипенем, меропенем.
а. экстракорпоральные методы детоксикации: серийный лечебный плазмаферез (после восполнения ОЦК и при отсутствии эндотоксинового шока) с плазмозаменой (1-3 сеанса через 24-48 часов, средний объем плазмоэксфузии не менее 1 л);
б. низкопоточная ультрадиафильтрапия при: сохраняющейся олигурии менее 500 мл/сутки, гиперкалиемии более 6,5 мэкв/л, скорости клубочковой фильтрации менее 20 мл/мин, увеличении уровня креатинина.
в. процесс детоксикации при тяжелом ОП может также достигаться путем эвакуации перитонеального, а особенно ретроперитонеального экссудата и проточно-промывного дренирования брюшной полости и забрюшинной клетчатки двухпросветными дренажами.
Протокол лапароскопической операции
Лапароскопия показана:
- пациентам с перитонеальным синдромом, в том числе при наличии УЗИ-признаков свободной жидкости в брюшной полости;
- при необходимости дифференцировки диагноза с другими заболеваниями органов брюшной полости.
Задачи лапароскопической операции могут быть диагностическими, прогностическими и лечебными.
Задачи лапароскопической операции:
подтверждение диагноза острого панкреатита (и, соответственно, исключение других заболеваний брюшной полости, прежде всего острой хирургической патологии — мезентериального тромбоза и др.).
К признакам ОП относятся:
- наличие отека корня брыжейки поперечной ободочной кишки;
- наличие выпота с высокой активностью амилазы (в 2-3 раза превышающей активность амилазы крови);
- 3. наличие стеатонекрозов;
выявление признаков тяжелого панкреатита:
- геморрагический характер ферментативного выпота (розовый, малиновый, вишневый, коричневый);
- распространенные очаги стеатонекрозов;
- обширное геморрагическое пропитывание забрюшинной клетчатки, выходящее за пределы зоны поджелудочной железы.
Верификация серозного отека в первые часы заболевания (особенно на фоне тяжелого общего состояния пациента) не исключает наличия тяжелого панкреатита, так как при лапароскопии в ранние сроки признаки тяжелого панкреатита могут не выявляться, т.е. заболевание в дальнейшем может прогрессировать.
лечебные задачи:
- удаление перитонеального экссудата и дренирование брюшной полости;
- лапароскопическая декомпрессия забрюшинной клетчатки (показана в случаях распространения геморрагического пропитывания на забрюшинную клетчатку вдоль восходящей и нисходящей ободочных кишок в зонах максимального поражения);
- холецистостомия показана при наличии прогрессирующей билиарной гипертензии с гипербилирубинемией более 100 мкмоль/л и не ранее чем через 24 часа от начала интенсивной терапии.
- При сочетании острого панкреатита с деструктивным холециститом показана в дополнение к перечисленным мероприятиям холецистэктомии с дренированием холедоха;
Лапароскопия противопоказана при:
- нестабильной гемодинамике (эндотоксиновом шоке);
- после множественных операций на брюшной полости (выраженном рубцовом процессе передней брюшной стенки и гигантских вентральных грыжах).
Протокол диагностики и лечения острого панкреатита в реактивной фазе
Диагностика и мониторинг перипанкреатического инфильтрата
Реактивная (промежуточная) фаза занимает вторую неделю заболевания, когда вследствие асептической воспалительной реакции на очаги некроза в поджелудочной железе и парапанкреатической клетчатке формируется перипанкреатический инфильтрат.
В клинической картине этого периода преобладают признаки системной воспалительной реакции — резорбтивная лихорадка, лейкоцитоз со сдвигом формулы влево, относительная лимфопения, увеличение СОЭ, повышение концентрации фибриногена, С-реактивного белка. УЗИ-признаками перипанкреатического инфильтрата являются сохраняющееся увеличение размеров поджелудочной железы, нечеткость ее контуров и появление жидкости в парапанкреатической клетчатке.
Мониторинг перипанкреатического инфильтрата включает ежедневную оценку изменений клинической картины и анализ данных лабораторных и УЗ-исследований, выполняемых в этот период не реже двух раз в неделю. В конце второй недели заболевания целесообразно выполнить компьютерную томографию зоны поджелудочной железы, так как к этому сроку у подавляющего большинства пациентов наблюдается один из трех возможных исходов реактивной фазы:
- рассасывание инфильтрата, при котором наблюдается редукция местных и общих проявлений острой воспалительной реакции;
- сохранение размеров перипанкреатического инфильтрата при нормализации самочувствия и стихании синдрома системной воспалительной реакции на фоне сохраняющейся гиперамилаземии;
- асептическая секвестрация панкреонекроза с исходом в кисту поджелудочной железы;
- септическая секвестрация (развитие гнойных осложнений).
Лечение перипанкреатического инфильтрата
У подавляющего большинства пациентов лечение острого панкреатита в реактивной фазе является консервативным. Лапаротомия на второй неделе выполняется только при осложнениях хирургического профиля (деструктивный холецистит, желудочно-кишечное кровотечение, острая кишечная непроходимость и др.), которые невозможно устранить эндоскопическими методами.
Лечение в этот период включает:
Лечебное питание (стол № 5а при среднетяжелом ОП) или энтеральную нутритивную поддержку (под контролем уровня амилаземии).
- Продолжение базисной инфузионно-трансфузионной терапии, направленной на восполнение водноэлектролитных, энергетических и белковых потерь.
- Системную антибиотикотерапию (цефалоспорины III-IV поколений или фторхинолоны П-Ш поколений в сочетании с метронидазолом, препараты резерва — карбапенемы).
- Иммуномодуляцию (два подкожных или внутривенных введения ронколейкина но 250 000 ЕД (при массе не менее 70 кг) — 500 000 ЕД (при массе более 70 кг) с интервалом в 2-3 дня).
Протокол диагностики и лечения острого панкреатита в фазе гнойных осложнений
Диагностика гнойных осложнений острого панкреатита
Клинической формой острого деструктивного панкреатита в фазе септического расплавления и секвестрации (третья неделя от начала заболевания и более) являются инфицированный панкреонекроз и гнойно-некротический парапанкреатит различной степени распространенности.
При компьютерной томографии и УЗИ органов брюшной полости отмечают увеличение числа и размеров жидкостных образований, появление девитализированных тканей (секвестров) и/или наличие пузырьков газа. О септическом воспалении свидетельствуют и положительные результаты бактериоскопии и бактериологического посева аспирата, полученного при тонкоигольной биопсии.
Решение о наличии у пациентов гнойных осложнений принимается на основании лабораторно-клинического минимума. Остальные признаки являются дополнительными.
Лечение гнойных осложнений острого панкреатита
- При гнойных осложнениях острого деструктивного панкреатита (ОДП) показано хирургическое вмешательство, целью которого является санация пораженной забрюшинной клетчатки. Объект оперативного вмешательства — гнойно-некротический парапанкреатит и/или инфицированный панкреонекроз. Операция включает раскрытие, санацию и дренирование пораженной забрюшинной клетчатки.
Основным методом санации гнойно-некротических очагов является некро-секвестрэктомия, которая может быть как одномоментной, так и многоэтапной, при этом целесообразно использовать миниинвазивные методы (пункция и дренирование под УЗИ и КТ-наведением; динамическая лапароскопия).
- В послеоперационном периоде показана комплексная терапия:
1. энтеральная нутритивная поддержка (через зонд, заведенный в тонкую кишку за связку Трейтца);
2. системная антибиотикотерапия (выбор антибактериального препарата зависит от чувствительности выделенных микроорганизмов) в сочетании с профилактикой дисбактериоза и других осложнений;
3.иммунокоррекция, варианты которой определяются индивидуально в зависимости от клинико-лабораторных показателей;
4. при тяжелом сепсисе — заместительная терапия иммуноглобулинами для внутривенного введения в сочетании с применением гормонов;
5. при стойком и выраженном ССВР — антицитокиновая терапия (ингибиторы протеаз, эфферентные процедуры);
6. при низком абсолютном числе лимфоцитов периферической крови — цитокиновая терапия ронколейкином в дозе 250 000 — 1 000 000 ЕД до восстановления показателя (в среднем 2-5 введений).
Ситуация при выборе способа лечения больных со стерильным панкреонекрозом достаточно неоднозначна. Объективных критериев, позволяющих достоверно даже во время операции определить протяженность, а точнее объем некроза ПЖ, до настоящего времени нет.
Лапаротомное хирургическое вмешательство, предпринятое в экстренном порядке по поводу ферментативного перитонита в доинфекционную фазу заболевания, следует считать необоснованным лечебным мероприятием.
Показания для видеолапароскопических вмешательств следующие:
- уточнение факта панкреонекроза;
- оценка распространенности и характера панкреатогенного перитонита;
- выявление источника перитонита другой этиологии;
- ферментативный перитонит;
- выполнение лапароскопической холецистостомы;
- оментобурсостомия.
Чрескожные вмешательства под контролем УЗИ в стерильную фазу выполняют в следующих случаях:
- отграниченные жидкостные образования забрюшинного пространства;
- дренирование брюшной полости при ферментативном перитоните;
- наложение холецистостомы или холангиостомы при желчной гипертензии;
- бактериологическое и биохимическое исследование экссудата.
Основываясь на фазовом течении острого панкреатита и возникающих осложнений, применение малоинвазивных технологий возможно во все фазы. В первую фазу применение малоинвазивных технологий можно рассматривать как диапевтические манипуляции, в последующие стадии — как лечебные.
Тонкоигольное пункционное вмешательство позволяет определить наличие контаминации, оценить распространенность процесса деструкции и способствует выведению больного из эндотоксического шока. Полученный экссудат в обязательном порядке направляется на определение уровня амилазы, микробиологическое и цитологическое исследования.
Острые жидкостные скопления (содержащие высокую концентрацию панкреатических ферментов) не более 5 см (по данным УЗИ) желательно аспирировать тонкоигольной пункцией (диаметр иглы не менее 18G), возможна многократная аспирация.
При более объемных жидкостных скоплениях в полости малого сальника или забрюшинном пространстве при отсутствии инфицирования необходимо кратковременное дренирование не более 2 суток, просвет дренажей не менее 12-15 Fr (4-5 мм). Контроль за состоянием брюшной полости и забрюшинного пространства осуществлять ежедневным ультразвуковым сканированием, при затрудненной визуализации — рентгеновской компьютерной томографией или ЯМР-томографией.
В проведении дренирующих перкутанных операций обычно используются следующие методы: стилет-катетер (одноэтапный), двухэтапный, троакарный. Выбор методики дренирования должен производиться в зависимости от топографии и размеров патологического очага.
Так, если предполагается прохождение траектории через брюшную полость, необходимо применять первые две методики. Первичное дренирование осуществлять дренажами 12-15 Fr, на третьи-четвертые сутки производить замену дренажей с проcветом 16-18 Fr и далее до 30 Fr.
При дренировании забрюшинного пространства без контакта с брюшной полостью отдается предпочтение троакарному способу, позволяющему сразу установить дренажи большого диаметра через «гильзы» ретроперитонеостомы. В дальнейшем через ретроперитонеостомические отверстия осуществлять осмотр, санацию забрюшинного пространства и удаление секвестров корзинкой Дормиа.
Считаем целесообразным рассматривать следующие показания к пункционным и катетеризационным лечебным чрескожным вмешательствам при панкреатогенных органных и внеорганных жидкостных образованиях:
- Жидкостные скопления в сальниковой сумке, в области селезенки и в паракольном пространстве.
- Формирующиеся постнекротические псевдокисты.
- Сформированные псевдокисты при наличии небольших тканевых включений и при отсутствии интерпанкреатической гипертензии.
- Рецидивные и резидуальные псевдокисты и жидкостные скопления брюшной полости.
- Абсцессы поджелудочной железы.
- Наличие жидкости в забрюшинном пространстве.
Билиарная гипертензия
В первую очередь пункционно-катетеризационные методы применяются к пациентам с ИОДП с нарастающей полиорганной недостаточностью и крайне сомнительной переносимостью операции. Кроме того, применение малоинвазивных процедур позволяет ликвидировать септические проявления и в дальнейшем выбрать более подходящее время для оперативного вмешательства в условиях наступившей демаркации некротизированных тканей.
По мнению ряда авторов, противопоказаниями к пункционно-катетеризационному лечению следует считать:
- Крупные секвестры в полости кисты.
- Признаки кровотечения в полость кисты.
- Подозрение на кистозную опухоль.
- Признаки панкреатической гипертензии.
- «Организованный» панкреонекроз без жидкостного компонента.
- Распространенный перитонит.
Однако с некоторыми выводами авторов можно не согласиться. Так, по нашему мнению, сочетание управляемого чрескожного дренирования некротических очагов большого размера множественными дренажами большого диаметра, заменой дренажей, агрессивная ирригация очагов и некроэктомия через просвет ретроперитонеостом позволяет избежать открытых операций.
Из-за неодновременного созревания секвестров и, возможно, из-за неадекватного дренирования забрюшинного пространства после традиционных операций довольно часто встречается абсцедирование. Дренирование проводится под УЗ-наведением, и траектория введения дренажа определяется с учетом адекватности оттока отделяемого, возможности замены дренажа по необходимости.
В абсцессы объемом более 60 мл устанавливаем два дренажа и более. При наличии секвестров проводим замену на дренажи с большим просветом — до 30 Fr. Большой внутренний просвет дренажа позволяет удалить крупные фрагменты некротических тканей. Дренирование необходимо проводить сразу из различных точек, которые выбирают с учетом возможно большего охвата дренируемого объема и адекватности дренирования.
Достоверно отмечено (с использованием прогностических систем Renson и APACHI-2) уменьшение частоты оперативных вмешательств в группе больных, где использовались навигационные технологии, по сравнению с группой больных, которым применялась традиционная хирургическая тактика.
При стерильном панкреонекрозе открытая операция является вынужденной мерой, когда исчерпан весь детоксикационный потенциал комплексных консервативных мероприятий и малоинвазивных вмешательств, однако возникают ситуации, являющиеся показаниями к проведению лапаротомии на 1 или 2 недели заболевания:
- сохранение и нарастание симптомов полиорганной недостаточности на фоне интенсивной терапии;
- неэффективность транскутанных и лапароскопических санационных вмешательств;
- подозрение на инфицирование.
Инфицированные формы панкреонекроза (инфицированный панкреонекроз, панкреатогенный абсцесс, флегмона забрюшинной клетчатки, гнойный перитонит, инфицированная киста) независимо от степени полиорганных нарушений требуют оперативного лечения. В противном случае фатальный исход заболевания неизбежен. Выбор метода операции в этом случае производят исходя из следующих критериев:
- характер и степень поражения поджелудочной железы;
- характер гнойно-некротического очага;
- топография гнойно-некротического очага;
- срок заболевания;
- степень тяжести состояния больного (APACHE II, Ranson, SOFA, SAPS).
Варианты хирургических вмешательств при инфицированном панкреонекрозе включают в себя открытые (лапаротомия, люмботомия) и закрытые вмешательства (чрескожные вмешательства под контролем УЗИ, видеолапароскопия).
При развитии ИП, когда по результатам УЗИ, КТ установлено, что некротический компонент очага существенно преобладает над жидкостным (либо последний вовсе отсутствует), а степень тяжести состояния больного не имеет тенденции к улучшению, применение чрескожных методов дренирование ограничено.
Цель, к которой стремится хирург, оперируя больного с ИП, обнаружить, санировать и дренировать все гнойно-некротические полости. Однако одномоментная санация у большинства больных с ИП не удается, это требует повторных вмешательств, так называемых программируемых санаций. Клинический смысл расчленения санаций на этапы основывается на следующих положениях:
- факт неодновременного созревания секвестров;
- вторичное прогрессирование гнойного процесса по типу затеков;
- большая опасность септического шока при одномоментном раскрытии обширных забрюшинных нагноений.
Программируемые санации обычно выполняются в режиме 24-72 часа или «по требованию», т.е. при возникновении экстренных показаний. После открытых хирургических вмешательств наиболее часто возникают следующие осложнения:
- аррозивные кровотечения — как правило, возникают в несанированных гнойно-некротических забрюшинных полостях. Чаще кровоточат сосуды mesocolon, селезеночная артерия и вена, панкреатодуоденальные сосуды;
- некрозы и свищи полых органов (перфорации острых язв, дуоденальные, тонкокишечные, толстокишечные свищи);
- системные осложнения (сепсис, ДВС-синдром, тромбоэмболия, пневмония).
В заключение необходимо подчеркнуть, что составляющие успеха ведения больных с острым панкреатитом, и особенно стерильным и инфицированным панкреонекрозом, должны включать современные представления о неразрывной патогенетической сущности этих состояний, определяющих стратегию топической диагностики и тактику комплексного лечения в неотложной панкреатологии.
Существует обоснованное мнение, что концентрация больных с панкреонекрозом в нескольких хирургических центрах, имеющих определенный опыт, квалифицированных специалистов и соответствующее оснащение, позволит кардинально улучшить результаты лечения острого панкреатита.
А.В. Абдульянов, А.З. Фаррахов, М.А. Бородин
Казанский государственный медицинский университет
Источник: http://pmarchive.ru/diagnostika-i-xirurgicheskoe-lechenie-bolnyx-destruktivnym-pankreatitom/
Деструктивный панкреатит
Панкреатит – серьёзное заболевание поджелудочной железы. Развитие боязни носит стремительный характер, что часто, особенно в случае промедления с лечением, чревато серьёзнейшими осложнениями. Острый деструктивный панкреатит или «панкреонекроз» — это осложнение острого панкреатита, возникающее вследствие развития воспалительного процесса в тканях поджелудочной железы, которое приводит к нарушению обменных процессов и отмиранию клеток этого органа.
Причины возникновения и развития болезни
Поджелудочная железа – важный и незаменимый орган, участвующий в пищеварительных процессах. Она производит три основных фермента:
- Липазу – отвечает за переваривание жиров, поступающих с пищей;
- Трипсин – отвечает за переваривание белков;
- Амилазу – отвечает за переработку углеводов.
Кроме того, орган производит гормоны, отвечающие за уровень сахара в крови человека.
Воспаление тканей поджелудочной железы, сужение либо закупорка панкреатических протоков приводит к тому, что пищеварительные ферменты не подпадают, как положено — в кишечник, а начинают свою пищеварительную активность в поджелудочной железе. В результате этого начинается процесс переваривания собственных тканей.
Кроме того, этот «пищеварительный» процесс выходит за пределы самой поджелудочной железы и затрагивает окружающие ткани и органы. Эти же ферменты попадают и в кровоток, в результате чего происходит поражение сердца, печени, почек, головного мозга, лёгких.
Формы и стадии развития
Под воздействием повреждающих факторов происходит отмирание клеток и тканей или, иначе говоря, некроз. По характеру и локализации повреждений железы деструктивный панкреатит бывает:
- Мелкоочаговым;
- Среднеочаговым;
- Крупноочаговым;
- Тотально-субтотальным – поражены все отделы поджелудочной железы (головка, тело, хвост).
Далее, если вовремя не обратиться за помощью, происходит возникновение гнойных образований под действием бактериальных токсинов и развитие абсцесса, как самой железы, так и окружающих тканей, и внутренних органов.
Болезнь характеризуется тяжёлым течением и при неблагоприятных обстоятельствах может наступить смерть пациента. Это может произойти как в первые дни после начала приступа в результате отказа жизненно важных органов и систем организма («ранняя смерть»), либо на третьей-четвёртой неделе («поздняя смерть») — в результате возникновения гнойно-септических осложнений.
Болезнь имеет три стадии развития
- Первая – ферментативная
На этом этапе начинается некротическое изменение ткани поджелудочной железы. Этот процесс происходит в течение трёх суток и носит название ферментативной фазы заболевания. Панкреатические ферменты выходят из ацинарных клеток и под действием фермента фосфолипазы А происходит разрушение клеточных мембран с последующим проникновением внутрь клеток железы фермента липазы. - Вторая стадия — реактивная
Эта фаза длится со второй по третью неделю с момента начала заболевания. Дальнейшее развитие болезни зависит от реакции организма на очаги некротического поражения. На таком этапе исход зависит от того, происходит ли рассасывание перипанкреатического инфильтрата, либо происходит образование кист и дальнейшее нагноение. - Третья стадия – секвестрационная
Начинается эта фаза с третьей недели с момента возникновения приступа и длится до нескольких месяцев. На этом этапе происходит образование свищей и кист без дальнейших осложнений (стерильный панкреонекроз), либо происходит дальнейшее усугубление ситуации, то есть развивается инфицированная форма панкреонекроза.
Это чрезвычайно опасная ситуация, когда возникают абсцессы, желудочно-кишечные кровотечения, перитонит и сепсис. На этой стадии очень велика вероятность летального исхода.
Причины возникновения болезни
Возникновение и развитие этой смертельно опасной болезни обусловлено рядом причин, основными из которых являются чрезмерное увлечение крепкими алкогольными напитками и патологии жёлчного пузыря.
Злоупотребление алкоголем. Это наиболее частая причина возникновения острого панкреатита. Как правило, возникает у людей, имеющих алкогольный стаж 5-15 лет, но не исключены случаи возникновения приступа после единичного случая употребления алкогольных напитков, в особенности в сочетании с жирной жареной пищей.
Желчнокаменная болезнь. В этом случае панкреатит развивается по причине закупорки жёлчным камнем сфинктера Одди, в результате чего желчь попадает через панкреатические протоки в поджелудочную железу. Либо имеет место закупорка желчным камнем панкреатических протоков и ферменты поджелудочной железы, не имея возможности попасть в кишечник, активируются в самой железе.
Кроме этого, известен и ряд других причин возникновения деструктивного панкреатита.
- Неконтролируемый приём лекарственных средств;
- Инфекционные и вирусные заболевания;
- Врождённые дефекты поджелудочной железы;
- Травмы поджелудочной железы;
- Неудачно проведенные операции и послеоперационные осложнения;
- Наличие паразитов в организме;
- Отравление химическими веществами и укусы ядовитых насекомых.
Симптоматика
Симптомы острого деструктивного панкреатита появляются в скором времени после обильного застолья с большим количеством алкоголя и жирной жареной мясной пищей либо в ночное время.
Возникновение приступа острого панкреатита характеризуется:
- Появлением острой и нестерпимой боли вверху живота. Она может локализоваться в правой части живота – если поражена головка поджелудочной железы, в левой – если хвост, и в центре – если поражение затронуло тело поджелудочной железы. При тотально-субтотальном повреждении боли носят опоясывающий характер. Болевые ощущения не снимаются обезболивающими препаратами.
- Возникновением тошноты и рвоты. Приступы рвоты носят затяжной и мучительный характер. Сначала – это съеденная ранее пища, затем – желчь. После приступа рвоты облегчение не наступает.
- Наличием признаков метеоризма и появлением диареи, что обусловлено недостатком ферментов, которые не попадают в кишечник для обеспечения процессов пищеварения.
В результате интоксикации происходит обезвоживание организма. Пациент ощущает сухость во рту. Далее с развитием болезни может наблюдаться:
- Покраснение лица;
- Повышение температуры;
- Учащение пульса;
- Одышка;
- Появление синюшных пятен на животе и ягодицах в результате повреждения сосудов;
- Пожелтение склер глаз и желтушный цвет лица в результате нарушения оттока жёлчи;
- Возникновение чувства страха;
- Потеря сознания.
Диагностика
Острый деструктивный панкреатит не имеет чёткой клинической картины, его симптомы схожи с симптомами других форм. Вследствие этого необходимо проведение тщательного исследования и диагностики. При подозрении на острый панкреатит больного доставляют в стационар для проведения обследования и оказания экстренной помощи.
Целью диагностики является:
- Определение фазы заболевания и степени поражения организма;
- Своевременное обнаружение осложнений;
- Выявление причин заболевания.
С этой целью проводятся:
- Лабораторные исследования крови и мочи;
- УЗИ – для определения размеров поджелудочной железы, исследования её формы и контуров, выявление наличия жидкости в забрюшинном пространстве;
- Рентгенологическое исследование – выявляет степень вздутия кишечника;
- Диагностическая лапароскопия – для определения наличия кровяных скоплений в полости и кровоизлияний по бокам брюшины;
- Компьютерная томография и магнитно-резонансная томография — помогают выявить участки некроза, определить состояние других внутренних органов.
Лечение
Лечение проводится в условиях стационара и направлено на следующие цели:
- Ликвидация болевых ощущений;
- Снятие спазмов протоков поджелудочной железы и воспаления;
- Обеспечение стабильной работы сердца;
- Снятие последствий интоксикации;
- Профилактика воспалительных процессов.
Хирургическое вмешательство предпринимается в случае отсутствии эффекта от консервативного лечения.
Деструктивный панкреатит – тяжёлое заболевание. Оно характеризуется высоким процентом смертности и инвалидности. Во избежание неприятностей необходимо пересмотреть отношение к алкоголю, а также вовремя проходить обследование на предмет других заболеваний внутренних органов, которые могут спровоцировать приступ острого панкреатита.
Источник: https://gastrotract.ru/bolezn/pankreatit/destruktivnyj-pankreatit.html
Острый деструктивный панкреатит
В последние десятилетия острый деструктивный панкреатит (ОДП) является одной из самых актуальных проблем в абдоминальной хирургии, особенно осложненные его формы.
По заключению ведущих экспертов различных стран и на основании статистических данных ВОЗ, отмечается тенденция к увеличению числа больных молодого и среднего возраста острым панкреатитом. Это является причиной не только медицинских, но и социально-экономических проблем, так как затрагивается преимущественно работоспособное население.
Увеличение заболеваемости связано, с одной стороны, особенностями режима питания, возрастающим злоупотреблением алкоголя и его суррогатов, распространенностью желчнокаменной болезни и, как следствие, увеличением абсолютного количества больных, а с другой стороны, улучшением клинико-лабораторной и инструментальной диагностики заболевания.
Среди этиологических факторов острого панкреатита наиболее значимыми являются желчнокаменная болезнь и алкогольная интоксикация. При механическом препятствии попадания желчи в двенадцатиперстную кишку, она может попасть в панкреатический проток, что активирует панкреатический сок. Данный факт приводит к разрушению протоковой системы поджелудочной железы и развитию некроза её паренхимы.
В результате алкогольной интоксикации происходит резкое нарушение жирового обмена, развивается первичная гиперлипидемия, которая играет важную роль в патогенезе острого панкреатита. Развивается нарушение транскапиллярного обмена, и алкоголь оказывает токсическое действие на стенку кровеносных сосудов.
Также причиной развития острого панкреатита могут быть травмы поджелудочной железы, операции в брюшной полости, инфекции (особенно у детей). Также панкреатиты могут развиться как осложнения различных заболеваний, которые сопровождаются расстройствами микроциркуляции. К ним можно отнести шок различной этиологии, эндокринные изменения, избыточное употребление лекарственных препаратов, опухоли поджелудочной железы.
Тяжесть и распространенность патологического процесса при ОДП зависят от сочетания патогенетических факторов, степени поражения ацинозных клеток, количества выделенной цитокиназы, степени активации протеаз и функционального состояния поджелудочной железы.
В литературе имеется клиническая концепция и теория патогенеза ОДП, разработанная В.С. Савельевым и соавт.. Выделены следующие положения:
- ведущая патобиохимическая роль в развитии заболевания принадлежит липолитической и протеолитической системам ферментов поджелудочной железы, калликреин-кининовой, плазминовой, тромбиновой, а также симпатико-адреналовой системам;
- панкреатогенная токсемия сопровождается глубокими нарушениями центральной и периферической гемодинамики;
- очаги панкреонекробиоза и воспалительная демаркационная реакция первично асептичны.
Для ферментативной фазы, длящейся первую неделю с момента начала заболевания и сопровождающейся асептическим некрозом, характерно развитие панкреатогенного шока и полиорганной недостаточности на фоне тяжелой интоксикации и выраженных гемодинамических нарушений.
При развитии реактивной фазы с формированием секвестров, исходы могут зависеть от присоединения инфекции. Для нее характерно возникновение гнойных осложнений вплоть до сепсиса. Известно, что гнойные осложнения возникают в 40-70% случаев, причем летальность при этом в 2-3 раза выше, чем при стерильном панкреонекрозе и составляет 70-85%.
Дальнейшая разработка проблемы гнойных осложнений панкреонекроза не только имеет научное значение, но и является практической необходимостью. В этом направлении целесообразно усовершенствование техники хирургических вмешательств. В настоящее время верификация масштаба некроза в железе и забрюшинном пространстве в основном осуществляется посредством ультразвукового исследования и компьютерной томографии.
Во многом, тактические подходы хирургического ведения больных основаны на уже имеющемся поражении в поджелудочной железе, брюшной полости и забрюшинном пространстве. При этом отсутствует индивидуальный прогноз в отношении возможных путей дальнейшего распространения патологического процесса.
В зависимости от локализации первоначального повреждения протоковой системы поджелудочной железы нами уточнялись варианты поражения клетчатки забрюшинного пространства, причем дальнейшая разработка данного направления исследований представляется актуальной.
Диагноз подтверждается специальными методами исследования, к которым относятся эндоскопическая ретроградная панкреатохолангиография, лапароскопия, компьютерная томография. Объем панкреонекроза (патоморфологический критерий) оценивается путем определения клинико-лабораторных проявлений токсикоза, куда входят показатели гемодинамики, диуреза, лейкоцитоза, среднемолекулярных пептидов в плазме крови, системной гипоксии и системной сосудистой проницаемости; иммунологических показателей — содержание Т-лимфоцитов.
А также концентрация интерлейкинов, фагоцитарного числа и другие; специфических маркеров некроза (метгемальбумин, щелочная фосфатаза, фибронектин, прекальцитонин, факторы роста гепатоцитов); рентгенологических признаков деструкции, ультразвукового исследования (УЗИ), компьютерной томографии (КТ); прямыми методами (лапароскопия или интраоперационно).
Динамика развития патологического процесса в поджелудочной железе при деструктивном панкреатите устанавливается с помощью ультразвукового исследования и компьютерной томографии. Их применение значительно улучшает диагностику острого панкреатита и являются «золотым стандартом» в диагностике панкреатита и его осложнений. Информативность УЗИ по данным различных авторов составляет 92-94,5%.
Рентгенологическое исследование живота позволяет определить уровень жидкости в проекции луковицы двенадцатиперстной кишки, симптом «дежурной петли», симптом «вырезанной» или «отрезанной» петли ободочной кишки, увеличение расстояния между желудком и поперечной ободочной кишкой, затемнение верхней половины брюшной полости, смещение содержащего газ желудка вперед.
Эндоскопическая ретроградная холецистопанкреатография позволяет получить детальное рентгеновское изображение протоковой системы железы с характерными патологическими изменениями. Селективная ангиография чревного ствола (целиакография) поджелудочной железы при остром панкреатите позволяет выявить признаки нарушения артериального кровотока в сосудах, кровоснабжающих поджелудочную железу.
Из общего анализа крови можно выявить лейкоцитоз, сдвиг лейкоцитарной формулы влево. Лейкоцитарный индекс интоксикации повышается в первые сутки заболевания, затем наступает постепенное его снижение до нормы. Как правило, чем тяжелее форма панкреонекроза, тем медленнее снижается данный показатель.
В последние годы исследователи обращают внимание на генетическую предрасположенность к тяжелым формам заболевания. При этом применяют молекулярно-генетические методы исследования с выявлением групп больных, у которых определяют склонность к развитию тяжелых форм острого панкреатита с септическими осложнениями.
Многие работы посвящены выявлению полиморфизма генов при хроническом и остром панкреатите. При анализе факторов, влияющих на развитие хронического панкреатита, выявили мутации в гене муковисцидоза (CFTR — сystic fibrosis transmembrane conductance regulator), панкреатический секреторный ингибитор трипсина.
В литературе описаны и другие мутации в генах, оказывающие влияние на состояние поджелудочной железы — SPINK1 (serine protease inhibitor kazal type 1), гены, отвечающие за синтез алкогольдегидрогеназы и альфа-1-антитрипсина. В развитии тяжелых форм панкреатита авторы отмечают роль полиморфизма в генах TNF-2 и TNF-alpha (tumor necrosis factor) и IL-8. Описан способ определения тяжести острого идиопатического панкреатита, основанный на обнаружении гетерозиготных мутаций в генах SPINK1, PRSS1 и CFTR.
В развитии острого панкреатита отмечают участие цитокинов, в частности ИЛ-1, ИЛ-6, ИЛ-10, ФАТ (фактор активации тромбоцитов). Доказано, что они имеют большое значение в начальных стадиях заболевания, и низкий их уровень свидетельствует о слабой выраженности воспалительной реакции, что прогностически неблагоприятно.
Для оценки степени тяжести состояния больных используются прогностические системы, основанные на клинических и лабораторных данных. Качественный способ прогнозирования основывается на индивидуальности тяжести острого панкреатита и заключается в выявлении специфических маркеров тяжелого панкреатита.
Современные системы объективной оценки тяжести состояния больных классифицируют следующим образом:
- Системы, оценивающие тяжесть состояния больных по количеству и сложности методов исследования и лечения, необходимых для его проведения (TISS).
- Методы, основанные на сборе объективных клинических показателей и лабораторных данных (APACHE, SAPS).
- Методы, основанные на статистическом моделировании (ИПМ)
Система TISS (Therapeutic Intervention Scoring System) оценивает тяжесть состояния больных по количеству и сложности методов исследования и лечения. При этом все диагностические и лечебные мероприятия делятся на 4 группы.
К первой группе относятся больные, требующие наблюдения и ухода. Для второй группы больных предусмотрены профилактические мероприятия. К третьей группе относятся больные, нуждающиеся в мониторинге и интенсивной терапии силами медицинских сестер. Больным четвертой группы показана интенсивная терапия бригадой врачей и медицинских сестер.
Балльная оценка тяжести заболевания по АРАСНЕ II (Acute Physiology and Chronic Health Evaluation) предполагает создание квалификационных групп больных. Она основана на воспроизведении данных измерений физиологических и лабораторных параметров, которые проводятся на раннем этапе пребывания больного в отделении интенсивной терапии.
Мангеймовский перитонеальный индекс был разработан специально для прогнозирования исхода перитонита. Эта шкала, по данным различных авторов, обладает высокой чувствительностью и точностью в оценке тяжести течения и прогноза заболевания. При этом возможен ретроспективный анализ случая, так как для этого требуется только стандартная информация.
Способ расчета коэффициента тяжести острого панкреатита, разработанный А.Н. Щербюком (1991), достаточно прост в применении и не занимает много времени. Данная система была разработана для определения сроков голодания при остром панкреатите.
В более ранних работах нами освещены вопросы ретроспективной оценки тяжести ОДП, с описанием способа оценки тяжести острого панкреатита. Последний основан на анатомическом анализе с учетом клинических проявлений болезни и статистического моделирования с определением возраста обследуемого, пола, наличия органной недостаточности, патологических изменений в поджелудочной железе, гнойно-некротических процессов в забрюшинной клетчатке.
При этом учитывают распространенность перитонита, его продолжительность, характер экссудата, а каждый показатель оценивают в баллах. Результаты оценки тяжести ОДП заносились в протокол аутопсии.
Довольно распространенной системой интегральной оценки степени тяжести состояния больного и прогноза острого панкреатита является шкала Ranson. По нему, в зависимости от количества критериев, возможно определение процента летальности в определенной группе больных.
Система SAPS II (Simplified Acute Physiology Score) содержит критерии, включающие физиологические параметры, возраст, экстренность поступления, предшествующие заболевания. Эта система обеспечивает оценку вероятности летального исхода без учета первичного диагноза.
Индекс «поражения» брюшной полости применяется для оценки тяжести состояния больного и эффективности проводимого лечения. На основании полученных интраоперационных и инструментальных данных рассчитывается индекс поражения поджелудочной железы, забрюшинного пространства и брюшной полости.
В начальный период острого панкреатита лечение направлено на купирование гнойно-некротических процессов в самой поджелудочной железе, предупреждение и снятие синдрома панкреатогенной токсемии, профилактику дальнейшего развития гнойно-септических осложнений.
Консервативное лечение осуществляется в условиях отделения реанимации и интенсивной терапии. Назначение ингибиторов протеаз сочетается с применением цитостатических препаратов, так как они угнетают синтез белка. Возможно эффективное лечение панкреатита соматостатином и его аналогами, снижающими панкреатическую секрецию, частоту осложнений и летальность.
В настоящее время широко используется концепция «обрыва» панкреонекроза, которая включает применение антиферментной терапии (октреотид), выведение из организма ферментативных токсинов (форсированный диурез, плазмаферез) и микродренирование брюшной полости. Данная концепция совершенствуется и претерпевает изменения. Нередко используется регионарное трансаортальное введение левокарнитина и сулодексида.
Оптимальным считается сочетание афферентной и эфферентной методик, когда возможно достижение нулевой летальности при лечении тяжелого панкреатита. На практике используется энергия низкочастотных ультразвуковых колебаний для удаления очагов некроза в поджелудочной железе и парапанкреатической клетчатке после их формирования, но до развития гнойно-септических осложнений.
Хорошо зарекомендовало себя применение гальванизации поджелудочной железы при лечении панкреатита. Признаки нарушения эвакуации секрета поджелудочной железы при остром панкреатите подталкивают на выполнение одномоментного наружного дренирования панкреатического протока с помощью фиброгастродуоденоскопии.
Острый панкреатит в зависимости от этиологического фактора делят (В.С. Савельев и соавт., 1983) на дуоденобилиарный, холецистогенный, контактный, ангиогенный, посттравматический, криптогенный и другие.
В США используется классификация (Атланта, 1992) по клиническим проявлениям, что предполагает наличие следующих вариантов острого панкреатита: острый панкреатит средней степени тяжести; острый панкреатит с тяжелым течением; острые жидкостные образования; панкреонекроз стерильный и инфицированный; острая псевдокиста; панкреатогенный абсцесс.
Острый панкреатит классифицируют по степени тяжести (легкая, средняя тяжелая, крайне тяжелая). По распространенности острого панкреатита определяют наличие локальной, субтотальной и тотальной форм. При этом выделены период гемодинамических нарушений (1-3 суток), функциональной недостаточности паренхиматозных органов (5-7 суток) и постнекротических осложнений (3-4 недели).
Несмотря на многочисленные этиологические факторы, лишь в 60-80% случаев устанавливается истинная причина ОДП. В остальных случаях говорят об «идиопатическом» панкреатите.
По фазам морфологических изменений острый панкреатит подразделяется на отечный (серозный, серозно-геморрагический), некротический (геморрагический, жировой, смешанный) и гнойный панкреатиты (первично гнойный, вторично гнойный, обострение хронического гнойного панкреатита).
При различных клинико-морфологических формах панкреонекроза имеются определенные различия. При отечном панкреатите поджелудочная железа увеличивается в размерах. Она становится бледной, «стекловидной». При гистологическом исследовании выявляется интерстициальный и внутриклеточный отек, дистрофические изменения ацинарных клеток.
При геморрагическом панкреонекрозе имеет место резкое увеличение размеров поджелудочной железы. Причем вначале возникает геморрагическое пропитывание окружающей клетчатки. По мере прогрессирования заболевания орган становится плотным, синюшно-красноватым, рисунок строения сохраняется лишь частично.
При жировом панкреонекрозе происходит развитие очагов жирового некроза различной величины преимущественно в местах скопления нейтрального жира. Очаги жирового панкреонекроза вначале появляются в самой железе, затем распространяются в перипанкреатические области.
При жировом панкреонекрозе, в отличие от предыдущей формы, зоны протеолитического распада характеризуются выраженным лейкотаксисом. При этом отмечается интенсивная миграция полиморфноядерных лейкоцитов в очаги липолитических повреждений ацинарной и жировой ткани.
За счет вовлечения в патологический процесс парапанкреатической жировой ткани происходит увеличение границ деструкции поджелудочной железы. Некротизированные ткани расплавляются с формированием абсцессов, которые в начале процесса асептичны, а затем приобретают бактериальный характер.
Таким образом, проблема острого панкреатита не теряет свою актуальность, несмотря на достижение успехов в его диагностике и лечении. На практике часто встречаются инфицированные формы болезни, характеризующиеся высокой интоксикацией организма и диффузным, без четких границ распространением инфекционного процесса по забрюшинной клетчатке.
Целесообразно более тщательное исследование путей распространения патологического процесса за пределы поджелудочной железы с учетом этапности их возникновения. Важно изучение генетической предрасположенности лиц к возникновению гнойно-некротических форм заболевания в корреляции с типом ОДП.
Четкий и полный клинико-анатомический анализ ОДП позволит выйти на более качественный уровень оказания медицинской помощи данной категории больных.
Источник: http://www.ambu03.ru/ostryj-destruktivnyj-pankreatit/